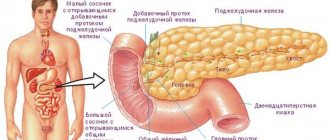
Каждый человек хотя бы единожды сталкивался с больными сахарным диабетом и знает, что эта патология требует заместительной терапии специальным веществом – инсулином. Но что такое инсулин, и почему он благотворно воздействует при высоком сахаре в крови?
Инсулин (гормон) – биологически активное вещество белковой природы, вырабатываемое поджелудочной железой для регуляции обмена веществ в тканях. В основном этот гормон отвечает за снижение уровня глюкозы крови за счёт ускорения синтеза гликогена.
Структура и состав белка
Инсулин — это гормон белковой природы. Молекулярная структура этого белка состоит из двух полипептидных цепей, которые образуются из аминокислотных остатков. Суммарно обе цепи содержат 51 остатков аминокислот: 21 из них содержится в А-цепочке, 30 – в В. Впервые точную последовательность аминокислотных частей определил английский молекулярный биолог Фредерик Сенгер.
Между собой цепи соединяются двумя ковалентными связями между атомами серы (дисульфидными мостиками), которые входят в состав аминокислоты цистеина. Ещё одна дисульфидная связь содержится в меньшей цепи инсулина. Пространственное строение вещества было определено с помощью метода рентгеновской дифракции биологом Дороти Кроуфут-Ходжкин.
Инсулин не только стал первым гормоном, для которого была определена полная первичная структура, но и до сих пор является наиболее изученным из всех продуктов желез внутренней секреции.
Структура инсулина у животных схожа, однако даже небольшие различия влияют на восприятие гормона человеком. Например, гормон, регулирующий уровень глюкозы в организме свиньи, отличается всего одним аминокислотным остатком, расположенным в концевом (30-ом) положении В-цепи, а именно аланином, который заменяет треонин.
Инсулин животных, относящихся к крупному рогатому скоту (например, бычий), отличается тремя аминокислотами. Белок, продуцируемый другими животными (в т.ч. китовый) ещё менее схож по первичной структуре.

Из-за содержания чужеродных аминокислотных остатков инсулин других биологических видов способен вызывать аллергическую реакцию. Её интенсивность зависит от степени различия белков.
Как происходит регуляция уровня глюкозы
Бета-клетки реагируют на содержание глюкозы в крови. При повышении уровня глюкозы бета-клетки стимулируют выработку инсулина. К количеству глюкозы особенно чувствительны инсулинозависимые мышечная и жировая ткани. На них приходится порядка двух третей клеточной массы в человеческом теле.
Если инсулин — это гормон поджелудочной железы, выполняющий функцию снижения уровня глюкозы в крови, то все остальные гормоны выполняют противоположную функцию, увеличивая его.
Гормональное регулирование также осуществляют:
- глюкагон;
- адреналин;
- глюкокортикоиды;
- соматотропин.
Помимо важнейшей задачи по снижению уровня сахара, действие инсулина на организм следующее:
- Повышает проницаемость клеток для проникновения в них глюкозы.
- Способствует усвоению белков.
- Обеспечивает синтез жирных кислот в печени.
- Помогает регенерационным процессам.
- Помогает усвоению микроэлементов.
- Препятствует попаданию жирных кислот в кровоток.
Как продуцируется этот гормон?
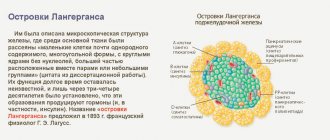
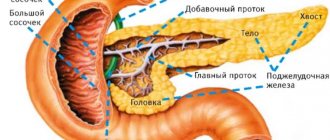
Инсулин вырабатывается в определённых образованиях поджелудочной железы, называемых островками Лангерганса-Соболевского (иногда упоминается только первый исследователь). Это объясняет этимологию названия гормона: в переводе латинское слово Insula означает «остров».
Изначально синтез инсулина кодируется геном, находящимся в коротком плече одиннадцатой хромосомы. Однако вырабатываемое на рибосомах пептидное вещество является предшественником проинсулина – т.н. невызревшей формы гормона. Кроме необходимых А и В-цепей, молекула предпроинсулина содержит L- и C-пептиды, состоящие, соответственно, из 24-х и 31-ого остатков аминокислот.
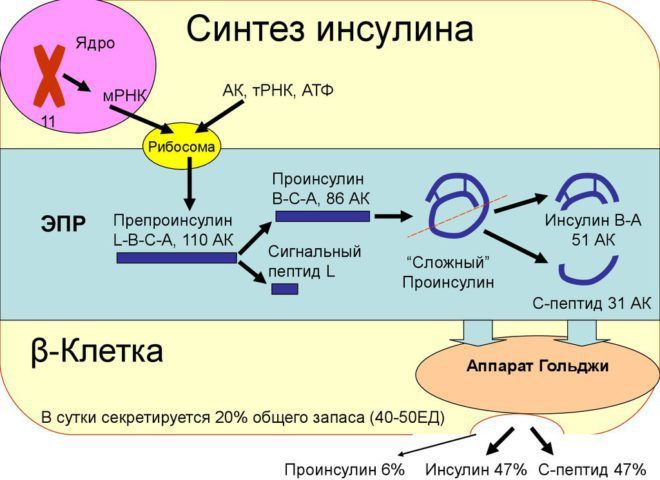
L-цепочка необходима для свободного прохождения синтезированного гормона сквозь липидный барьер (мембрану), поэтому проинсулин образуется практически сразу же после синтеза предшественника.
После этого молекулы образованного вещества транспортируются в комплекс Гольджи, в котором происходит т.н. вызревание инсулина. Этот этап является наиболее длительным в процессе образования активного гормона. При созревании из структуры проинсулина вырезается С-цепочка, которая соединяет А- и В-пептиды: таким образом, молекулы разделяются на инертный остаток и инсулин.
Готовое вещество хранится в секреторных гранулах островков Лангерганса: соединяясь с активными ионами цинка, инсулин образует твёрдые гексамерные агрегаты с кристаллическим строением.
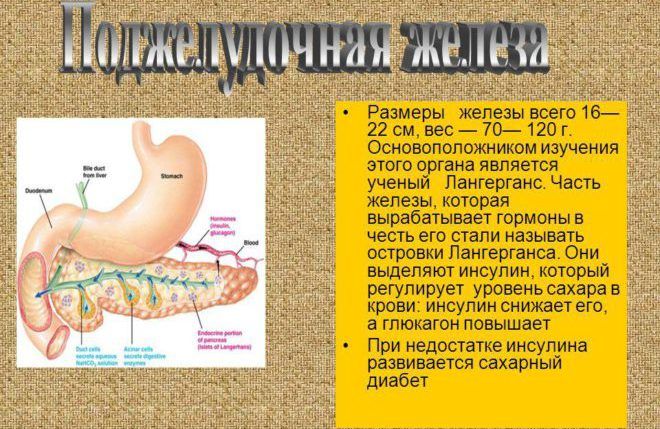
Бета-клетки этих образований чувствительны к повышению концентрации глюкозы в кровяном русле. Секреция гормона инсулина поджелудочной железой происходит поэтапно:
- Глюкоза транспортируется в β-клетки специальным белком.
- Моносахарид окисляется с образованием АТФ (вещества, являющегося источником энергии для систем организма). Количество синтезированного АТФ зависит от количества глюкозы.
- Образованная АТФ стимулирует закрытие калиевых каналов клеток и открытию кальциевых.
- Повышение содержание кальция активирует один из видов фосфолипаз, что приводит к ещё большему росту концентрации кальция в клетке.
- Резкое увеличение количества ионов кальция стимулирует высвобождение хранящегося в секреторных гранулах инсулина.
Гранула расщепляется во время прохождения плазматической мембраны. Изменение свойств среды приводит к отщеплению цинка и неактивных частей.
Когда инсулина избыток
Когда поджелудочная образует повышение гормона, клетками вырабатывается слишком большое количество вещества, что ведет к проблемам со здоровьем. Поэтому нужно снижать образующуюся производительность гормона в организме.
Образование поджелудочной выработки в большом объеме инсулина фиксируется, когда имеются тяжелые болезни печени, патологи Кушинга.
Не исключен тот случай, что при высоком показателе возникает стимулирование болезненных изменений, к примеру, поликистоз яичников у женщин. Характерным признаком заболевания поджелудочной становится усиленное откладывание жирового запаса в зоне брюшины, формируется абдоминальное ожирение.
При избытке показателя долго заживают раны, трещины, царапины, потому важно для больных диабетом не повреждать кожный покров. Ткани будут длительно восстанавливаться, болеть, раны воспаляться и гноиться. Также по такой схеме избыток показателя ведет к появлению гангрены ног по причине варикоза и трофических нарывов.
В случае завышенного показателя понижается глюкоза до минимума, больной столкнется с вспышками голода, частой пульсацией, учащенным биением сердца, обмороками.
Инсулин относится к гормону, регулирующий присутствие сахара, участвует в выработке энзимов. Если имеется расхождение с нормой, то это сигнализирует о присутствии заболевания, которое требует срочного устранения.
Содержание статьи:
Инсулин – белковый гормон, вырабатываемый поджелудочной железой. Его основная роль – транспортировать глюкозу в ткани организма и поддерживать её уровень в крови на оптимальном уровне. Недостаточная выработка инсулина приводит к нарушению процессов обмена в организме и развитию сахарного диабета. Как организовать правильное питание, чтобы предотвратить заболевание и какие продукты помогут поджелудочной железе вырабатывать инсулин, узнаем далее.
Функции пептидного гормона
Основные функции инсулина в теле человека:
- Усиление поглощения глюкозы и других необходимых веществ клетками инсулинозависимых органов (печень, мышечная ткань, жировая прослойка).
- Активация ферментов, играющих ключевые роли в окислении моносахарида. Многие из эффектов инсулина в организме человека реализуются исключительно благодаря свойству гормона влиять на активность ферментов.
- Усиление интенсивности производства гликогена – полисахарида, сохраняющего глюкозу в клетках печени и мышц для дальнейшего использования. Инсулин стимулирует запасание моносахарида путём его полимеризации.
- Угнетение глюконеогенеза (образования глюкозы в печени из белков и жирных кислот).
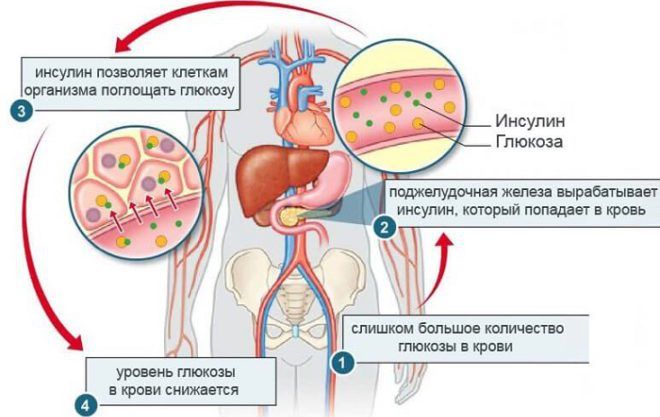
Схема выработки инсулина в организме
При недостатке инсулина сигналы контролирующего органа (мозга) стимулируют производство глюкозы из имеющихся запасов жировых кислот и белковой ткани. Процесс является энергетически невыгодным для организма, поэтому ткани, способные поглощать кетоновые тела, переводятся на этот источник питания, а образующаяся глюкоза поступает к мозгу и другим тканям, которые могут получать энергию только при окислении моносахарида.
Невозможность поглощения глюкозы клетками инсулинозависимых органов приводят к их голоданию и повышению синтеза кетоновых тел. Именно этим поясняется запах ацетона изо рта при недостатке углеводов в питании или патологиях, связанных с низкой выработкой инсулина. Повышение концентрации инсулина до приемлемого уровня в сочетании с полноценным питанием подавляет синтез кетоновых тел, оказывающих токсическое воздействие на ткани центральной нервной системы.
При большом количестве простых углеводов в питании сахар в крови повышается и снижается резко. Выработка инсулина и угнетение его секреции после снижения уровня глюкозы до приемлемого происходит с некоторой задержкой. В результате частые скачки концентрации гормона могут спровоцировать нарушение чувствительности тканей к инсулину, чего допускать крайне нежелательно.
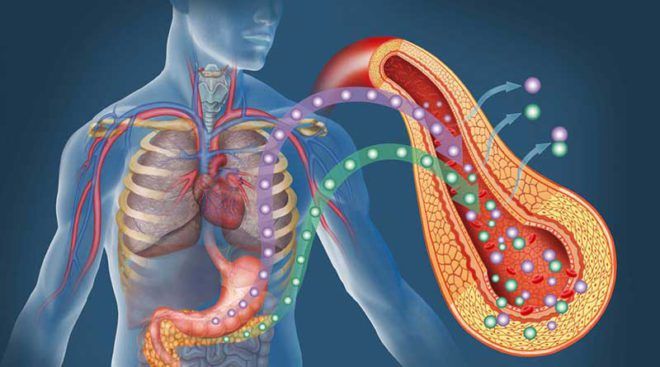
Функции инсулина в организме человека не ограничиваются регуляцией обмена глюкозы. Этот гормон оказывает также анаболическое и антикатаболическое действие: подавляет деградацию белков и расщепление жиров, усиливает поглощение некоторых аминокислот и транспорт ионов фосфата, магния и калия в клетки, стимулирует синтез белка и жирных кислот.
Профилактика заболеваний
Разобравшись, где вырабатывается инсулин, как происходит выработка инсулина и в организме человека, следует научиться предпринимать меры для профилактики заболеваний, связанных с поджелудочной железой.
Инсулин это гормон поджелудочной железы, у человека он образуется в ответ на повышение уровня сахара в кровотоке, таким образом, для предупреждения нарушений необходимо не допускать перепадов гликемии, придерживаться правил здорового питания.
Примечательно, что при грамотно подобранной диете удается восстановить работу ослабленного органа и поддерживать его естественную работу, чтобы не допустить проблем со здоровьем.
Эндокринологи и диетологи рекомендуют отказаться либо максимально ограничить вредную пищу, которая отрицательно сказывается на состоянии поджелудочной железы:
- полуфабрикаты;
- жареные блюда;
- консервация;
- сладости;
- острые специи.
Делать ставку нужно на свежие овощи, фрукты, натуральные несладкие фруктовые соки, злаки и молочные продукты. Улучшает работу организма, если в течение суток выпивать до 2.5 литров воды.
В разы облегчить функционирование поджелудочной железы помогает отказ от пагубных привычек, а именно курения и употребления алкогольными напитками. При длительном воздействии отрицательных факторов происходит мощное засорение организма токсическими веществами, человек страдает от беспричинных с первого взгляда гормональных сбоев, которые грозят не только сахарным диабетом, но и не менее опасными заболеваниями.
Врачи советуют время от времени проводить чистку организма от вредных веществ, проводить общее оздоровление, снижать негативное воздействие на поджелудочную железу. В этих целях показаны народные средства и лекарственные препараты, которые существенно упрощают задачу.
Нередко у пациентов диагностируют воспалительный процесс в органе (заболевание панкреатит), течение болезни неприятное, а исход может быть печальным. Воспаление может протекать в хронической и острой форме, отмечаются деструктивные процессы в тканях самого органа, препятствие работы почек, легких, печени, сердца и головного мозга.
При остром течении патологии есть угроза жизни пациента, воспаление возникает неожиданно, часто становится следствием:
- избыточного употребления спиртных напитков;
- присутствия камней в протоках.
Симптомами заболевания в таком случае будут: расстройство стула, рвотные позывы, приступы тошноты, мощный болевой синдром в спине, нижнем подреберье брюшной полости.
Если пациента беспокоят такие симптомы, ему необходимо отказаться от приема пищи и обратиться в поликлинику для диагностики организма.
Важно помнить, что клетки вырабатывающие инсулин погибают навсегда.
Нарушения, связанные с недостатком или переизбытком белка
К основным заболеваниям, которые так или иначе связаны с выработкой инсулина, относятся сахарный диабет, инсулинома и синдром хронической передозировки, характерный исключительно для пациентов, длительное время принимавших препараты этого гормона в избыточной дозе.
Сахарный диабет 1-го типа – это заболевание, характеризующееся аномально низкой выработкой инсулина и нарушением углеводного обмена как следствием основной патологии. Заболевание развивается из-за разрушения β-клеток поджелудочной железы иммунной системой пациента. На данный момент не существует активных методов лечения диабета 1-го типа, медикаментозные курсы ограничиваются контролем питания, поддерживающей инсулиновой терапией, приёмом витаминно-минеральных комплексов и общеукрепляющих антидиабетических препаратов.
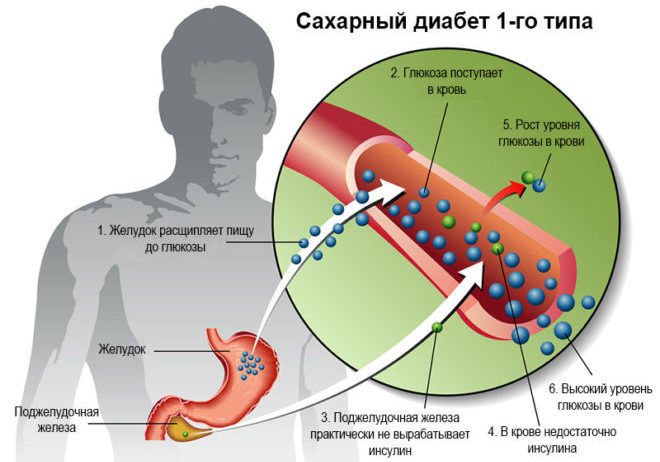
Не следует путать сахарный диабет 1-го и 2-го типов. В первом случае нарушение является следствием недостаточной выработки гормона, а во втором – пониженной чувствительностью инсулинозависимых тканей к его действию. При диабете второго типа в постоянной инсулиновой терапии часто нет необходимости.
При избытке введённого препарата у пациента может развиться инсулиновый шок – комплекс симптомов, указывающих на гипогликемию (чрезмерно низкий уровень глюкозы в крови). Чаще патологическое состояние, вызываемое избытком введённого инсулина, называется гипогликемической комой.
В течение нескольких минут после резкого падения уровня сахара крови может наступить потеря сознания, и даже паралич некоторых центров мозга. Из-за сильного воздействия на центральную нервную систему терапия инсулиновым шоком применялась в прошлом столетии для лечения некоторых психиатрических заболеваний.
Синдром Сомоджи, в отличие от инсулинового шока, возникает не при однократном введении избыточного количества инсулина, а при регулярном превышении дозировки гормона. В медицинской практике этот симптомокомплекс также носит название «синдрома хронической передозировки инсулина».

Инсулинома – это доброкачественное новообразование из бета-клеток железы, продуцирующей этот гормон. Опухолевая ткань вырабатывает избыточное количество инсулина, что чревато проявления всех симптомов гипогликемии, вплоть до потери сознания из-за недостатка глюкозы в тканях центральной нервной системы.
ДИАГНОСТИКА ФУНКЦИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
ПЕРЕЧЕНЬ ИССЛЕДОВАНИЙ:
- Инсулин (ИРИ)
- Аутоантитела к инсулину A-IAA
- С-пептид
- Лептин (гормон пищевого поведения)
- Гемоглобин гликозилированный (HbA1C)
- Холестерин
- Холестерин-ЛПВП
- Холестерин-ЛПНП
Лептин (Leptin)
Гормон, регулирующий энергетический обмен и массу тела
Лептин – пептидный гормон, который секретируется жировыми клетками и, как предполагается, участвует в регуляции энергетического обмена организма и массы тела. Он уменьшает аппетит, повышает расход энергии, изменяет метаболизм жиров и глюкозы, а также нейроэндокринную функцию либо прямым влиянием, либо активацией специфических структур в центральной нервной системе.
Содержание лептина в крови возрастает с увеличением тучности и снижается при уменьшении количества жировой ткани. В норме повышение уровня лептина подавляет секрецию в гипоталамусе нейропептида Y, участвующего в формировании чувства голода, и стимулирует активность симпатической нервной системы. Снижение уровня лептина после значительного похудания вызывает повышение аппетита и последующее восстановление веса (массы тела).
Изменения уровня лептина связывают с механизмами развития аменореи, обусловленной anorexia nervosa, bulimia nervosa, а также чрезмерными физическими нагрузками у женщин-атлетов. В этих ситуациях уровень лептина снижен.
Предполагается, что концентрация лептина играет роль физиологического сигнала о достаточности энергетических ресурсов организма для выполнения репродуктивной функции и влияет на стероидогенез в яичниках. В период пубертата происходит повышение концентрации в крови лептина.
Генетический дефицит лептина (синтез которого связан с ob-геном – геном тучности) при редких случаях наследственного дефицита лептина у людей вызывает патологическое ожирение, поддающееся лечению с применением экзогенного лептина.
В остальных случаях для тучных людей характерно, напротив, повышение концентрации лептина, которое не сопровождается соответствующим изменением пищевого поведения и энергетического обмена. Предположительно, это обусловлено «лептиновой резистентностью», которую связывают с нарушением переноса гормона транспортными белками или растворимыми рецепторами лептина. В настоящее время его рассматривают в качестве одного из факторов патогенеза инсулиннезависимого сахарного диабета. Избыток лептина приводит к подавлению секреции инсулина, вызывает резистентность скелетных мышц и жировой ткани к его воздействию, подавляет действие инсулина на клетки печени, что приводит к еще большему повышению уровня глюкозы при диабете II типа.
Однако само по себе ожирение при нормальной функции поджелудочной железы не приводит к диабету.
Кроме того, высокий уровень лептина создает высокую вероятность тромбоза. Исследования показывают, что тромб начинает образовываться в результате особого взаимодействия между лептином и рецепторами к нему, расположенными на тромбоцитах – клетках, ответственных за свертываемость крови.
Установлено, что связь между количеством лептина и заболеваниями сердечно-сосудистой системы существует вне зависимости от других факторов риска, таких как курение, наличия высокого уровня холестерина и высокого кровяного давления.
Показания к назначению анализа:
- Подозрение на генетический дефицит лептина (ранее возникновение выраженного ожирения);
- В комплексе исследований проблем повышения или снижения веса;
- Нарушения репродуктивной функции на фоне сниженного питания и чрезмерных физических нагрузок;
- В комплексе исследований, связанных с выявлением факторов риска сердечно-сосудистых заболеваний;
- Дифференциальная диагностика сахарного диабета типа II и ожирения;
- Рецидивирующие тромбозы.
Подготовка к анализу:
между последним приемом пищи и взятием крови проходит не менее 8 часов (желательно — не менее 12 часов). Сок, чай, кофе (тем более с сахаром) — не допускаются. Можно пить воду.
Материал: сыворотка или плазма крови (без гемолиза и липемии).
Единицы измерения: Единицы измерения в БиоТесте: нг/мл.
Референсные величины: Взрослые: Женщины – 1,1 – 27,6 нг/мл; Мужчины – 0,5 – 13,8 нг/мл.
Повышение значений лептина:
- Ожирение, инсулиннезависимый сахарный диабет;
- Усиленное питание.
Понижение значений лептина:
- Голодание;
- Снижение веса; (массы тела);
- Ожирение, связанное с генетическим дефицитом лептина.
С-Пептид (C-Peptide)
Биологически неактивный маркёр углеводного обмена, показатель секреции эндогенного инсулина.
С-пептид — устойчивый фрагмент эндогенно продуцируемого проинсулина, «отрезаемый» от него при образовании инсулина. Уровень С-пептида соответствует уровню инсулина, выработанного в организме.
В молекуле проинсулина между альфа- и бета-цепями находится фрагмент, состоящий из 31 аминокислотного остатка. Это так называемый соединительный пептид или C- пептид. При синтезе молекулы инсулина в бета-клетках поджелудочной железы этот белок вырезается пептидазами и вместе с инсулином попадает в кровоток. До отщепления С-пептида инсулин не активен. Это позволяет поджелудочной железе образовывать запасы инсулина в виде про-гормона. В отличие от инсулина С-пептид биологически неактивен. С-пептид и инсулин выделяются в эквимолярных количествах, поэтому определение уровня С-пептида позволяет оценить секрецию инсулина.
Надо отметить, что хотя количество образующихся при секреции в кровь молекул С-пептида и инсулина одинаково, молярная концентрация С-пептида в крови превышает примерно в 5 раз молярную концентрацию инсулина, что связано, по-видимому, с разной скоростью выведения этих веществ из кровотока. Измерение С-пептида имеет ряд преимуществ по сравнению с определением инсулина: период полураспада С-пептида в кровообращении больше, чем инсулина, поэтому уровень С-пептида — более стабильный показатель, чем концентрация инсулина. При иммунологическом анализе С-пептид не дает перекреста с инсулином, благодаря чему измерение С-пептида позволяет оценить секрецию инсулина даже на фоне приема экзогенного инсулина, а также в присутствии аутоантител к инсулину, что важно при обследовании больных с инсулинзависимым сахарным диабетом.
Уровень С-пептида изменяется в соответствии с колебаниями уровня инсулина, образующегося эндогенно. Соотношение этих показателей может изменяться на фоне заболеваний печени и почек, поскольку инсулин метаболизируется преимущественно печенью, а метаболизм и выведение С-пептида осуществляется почками. В связи с этим определение данного показателя может быть полезным для правильной интерпретации изменений содержания инсулина в крови при нарушении функции печени.
Показания к назначению анализа:
- Дифференциальная диагностика диабета 1 и 2 типов;
- Прогнозирование течения сахарного диабета;
- Бесплодие,синдром поликистозных яичников;
- Дифференциальная диагностика гипогликемических состояний;
- Подозрение на искусственную гипогликемию;
- Оценка остаточной функции бета-клеток у диабетиков на фоне инсулинотерапии;
- Выявление и контроль ремиссии (юношеский диабет);
- Диагностика инсулиномы;
- Оценка возможной патологии плода у беременных женщин, больных диабетом;
- Оценка секреции инсулина при заболеваниях печени;
- Контроль после удаления поджелудочной железы.
Подготовка к исследованию: натощак.
- Материал для исследования: сыворотка.
- Метод определения: твердофазный хемилюминесцентный иммуноанализ.
- Единицы измерения и коэффициенты пересчета: Единицы измерения в лаборатории БиоТест — пмоль/л
- Альтернативные единицы измерения — нг/мл; Перевод единиц: нг/мл х 331 ==> пмоль/л
Референсные значения: 298- 1324 пмоль/л
Повышение уровня С-пептида:
- Гипертрофия бета-клеток;
- Инсулинома;
- Антитела к инсулину;
- Инсулиннезависимый сахарный диабет (ИЗСД II типа);
- Гипогликемия при приеме пероральных сахароснижающих препаратов (производные сульфонилмочевины);
- Соматотропинома;
- APUDома;
- Почечная недостаточность; 9. Приём пищи; 10. Прием препаратов содержащих эстрогены, прогестерон, глюкокортикоиды, хлорохин, даназол, этинил-эстрадиол, пероральные контрацептивы.
Снижение уровня С-пептида:
- Инсулинзависимый сахарный диабет (ИЗСД I типа);
- Инсулинотерапия (нормальная реакция поджелудочной железы в ответ на введение экзогенного инсулина);
- Алкогольная гипогликемия;
- Состояние стресса;
Антитела к инсулиновым рецепторам (при инсулинорезистентном сахарном диабете II типа).
Гликированный гемоглобин (HbA1с)
Соединение гемоглобина с глюкозой, позволяющее оценивать уровень гликемии за 1- 3 месяца, предшествующие исследованию.
Образуется в результате медленного неферментативного присоединения глюкозы к гемоглобину А, содержащемуся в эритроцитах. Гликированный (употребляется также термин «гликозилированный») гемоглобин присутствует в крови и у здоровых людей.
Скорость этой реакции и количество образующегося гликированного гемоглобина зависят от среднего уровня глюкозы в крови на протяжении срока жизни эритроцитов. В результате реакции образуется несколько вариантов гликированных гемоглобинов: НbA1a, HbA1b, HbA1c. Последняя форма количественно преобладает и дает более тесную корреляцию со степенью выраженности сахарного диабета.
Гликированный гемоглобин отражает гипергликемию, имевшую место на протяжении периода жизни эритроцитов (до 120 суток). Эритроциты, циркулирующие в крови, имеют разный возраст. Обычно ориентируются на усредненный срок — 60 суток. Уровень гликированного гемоглобина является показателем компенсации углеводного обмена на протяжении этого периода. Нормализация уровня гликированного гемоглобина в крови происходит на 4-6-й неделе после достижения нормального уровня глюкозы. У больных сахарным диабетом уровень этого соединения может быть повышен в 2-3 раза.
В соответствии с рекомендациями ВОЗ этот тест признан оптимальным и необходимым для контроля сахарного диабета. Больным сахарным диабетом рекомендуется проводить исследование уровня гликированного гемоглобина не менее одного раза в квартал.
Значения могут различаться между лабораториями в зависимости от применяемого аналитического метода, поэтому контроль в динамике лучше проводить в одной лаборатории или, по крайней мере, тем же методом. При контроле над лечением диабета рекомендуется поддерживать уровень гликированного гемоглобина менее 7% и пересматривать терапию при содержании гликированного гемоглобина более 8% (указанные значения применимы только для сертифицированных методов определения гликированного гемоглобина с референсными пределами 4-6%).
Клинические исследования с использованием сертифицированных методов показывают, что рост доли гликированного гемоглобина на 1% связан с увеличением уровня глюкозы плазмы крови, в среднем, примерно на 2 ммоль/л. Гликированный гемоглобин используется как показатель риска развития осложнений диабета. Доказано, что снижение значений гликированного гемоглобина на 1/10 связано с примерно 45%-ным снижением риска прогрессии диабетической ретинопатии.
Результаты теста могут быть ложно изменены при любых состояниях, влияющих на средний срок жизни эритроцитов крови. Кровотечения или гемолиз вызывают ложное снижение результата; гемотрансфузии, естественно, искажают результат; при железодефицитной анемии наблюдается ложное повышение результата определения гликированного гемоглобина.
Показания к назначению анализа
Долговременный мониторинг течения и контроль над лечением больных сахарным диабетом для определения степени компенсации заболевания.
Подготовка к исследованию
Взятие крови желательно производить натощак. Исследование нецелесообразно проводить после кровотечений, гемотрансфузий.
- Материал для исследования: цельная кровь с антикоагулянтом (ЭДТА).
- Метод определения: боратный метод.
- Сроки исполнения: 1 рабочий день.
- Единицы измерения и коэффициенты пересчета: единицы измерения в лаборатории БиоТест — % от общего количества гемоглобина.
- Референсные значения: 4,5-6,5% от общего содержания гемоглобина.
Повышение значений HBA1c:
- Сахарный диабет и другие состояния с нарушенной толерантностью к глюкозе.
- Дефицит железа.
- Спленэктомия. Ложное повышение может быть обусловлено высокой концентрацией фетального гемоглобина (HbF).
Cнижение значений HBA1c:
- Гипогликемия.
- Гемолитическая анемия.
- Кровотечения.
- Переливание крови.
Нормальное содержание белка в крови
Выработка инсулина контролируется по содержанию глюкозы в крови. Нормальный уровень сахара для человека составляет до 5,4-5,6 ммоль/л. При результате в 5,6-6,6 ммоль/л врачи рекомендуют специальную диету с пониженным количеством углеводов (в особенности простых – сахара, хлеба, сладких фруктов и др.).
Если уровень сахара превышает 6,7 ммоль/л при соблюдённой технике проведения исследования, необходимо провести дополнительную диагностику и назначить адекватную противодиабетическую или иную терапию.
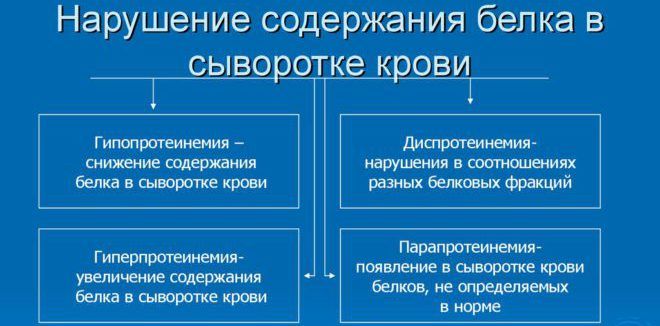
При повышенном сахаре пациенту назначается тест на толерантность к глюкозе. Нормальным результатом является 7,7 ммоль/л и ниже, промежуточное значение, свидетельствующее о нарушениях в работе обмена веществ, равняется 7,8-11,1 ммоль/л. Результат выше этих показателей говорит о диабете. Слишком низкие показатели могут говорить о недоедании или патологии. У детей пониженная концентрация глюкозы является вариантом нормы из-за недоразвитости центральной нервной системы и быстрого обмена веществ.
Кровь для исследования на уровень глюкозы берётся натощак или, по крайней мере, через полтора часа после последнего приёма пищи. Нарушение этого правила делает результат бесполезным для диагностики.
Непосредственно уровень инсулина исследуется редко, этот анализ является дополнительным методом диагностики. Нормальная концентрация гормона составляет 3-28 мкЕд/мл. Развитие плода провоцирует повышение уровня гормона в крови из-за взаимосвязи с гормоном роста, поэтому у беременных женщин результат может быть несколько выше (в среднем от 6 мкЕд/мл).

Изменение выработки инсулина — причины, симптомы и последствия
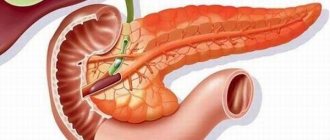
Поджелудочная железа — вторая по величине железа пищеварительной системы, ее масса 60-100 г, длина 15-22 см.
Эндокринная активность поджелудочной железы осуществляется островками Лангерганса, которые состоят из разного типа клеток. Примерно 60% островкового аппарата поджелудочной железы составляют β-клетки. Они продуцируют гормон инсулин, который влияет на все виды обмена веществ, но прежде всего снижает уровень глюкозы в плазме РєСЂРѕРІРё.
Таблица. Гормоны поджелудочной железы
Инсулин (полипептид) — это первый белок, полученный синтетически вне организма в 1921 г. Бейлисом и Банти.
Инсулин резко повышает проницаемость мембраны мышечных и жировых клеток для глюкозы. Вследствие этого скорость перехода глюкозы внутрь этих клеток увеличивается примерно в 20 раз по сравнению с переходом глюкозы в клетки в отсутствие инсулина. В мышечных клетках инсулин способствует синтезу гликогена из глюкозы, а в жировых клетках — жира. Под влиянием инсулина возрастает проницаемость клеточной мембраны и для аминокислот, из которых в клетках синтезируются белки.
Рис. Основные гормоны, влияющие на уровень глюкозы крови
Второй гормон поджелудочной железы глюкагон — выделяется а-клетками островков (примерно 20%). Глюкагон по химической природе полипептид, а по физиологическому воздействию антагонист инсулина. Глюкагон усиливает распад гликогена в печени и повышает уровень глюкозы в плазме крови. Глюкагон способствует мобилизации жира из жировых депо. Подобно глюкагону действует ряд гормонов: СТГ, глюкокортиконды, адреналин, тироксин.
Таблица. Основные эффекты инсулина и глюкагона
| Вид обмена | Инсулин | Глюкагон |
| Углеводный | Повышает проницаемость клеточных мембран для глюкозы и ее утилизацию (гликолиз) Стимулирует синтез гликогена Угнетает глюконеогенез Снижает уровень глюкозы крови | Стимулирует гликогенолиз и глюконеогенез Оказывает контринсулярное действие Повышает уровень глюкозы крови |
| Белковый | Стимулирует анаболизм | Стимулирует катаболизм |
| Жировой | Угнетает липолиз Уменьшается количество кетоновых тел в крови | Стимулирует липолиз Повышается количество кетоновых тел в крови |
Третий гормон поджелудочной железы — соматостатин выделяется 5-клетками (примерно 1-2%). Соматостатин подавляет освобождение глюкагона и всасывание глюкозы в кишечнике.
Выработка инсулина поджелудочной железой понижается по разнообразным причинам. Конечно, она прекращается из-за сбоя в функционировании органа. Поджелудочная перестает работать не просто так, есть определенная первопричина. Основная из них – вредная привычка, когда человек часто переедает, кушает еду с высокой калорийностью, в меню присутствуют продукты с большим объемом рафинированных углеводов.
Почему поджелудочная железа не вырабатывает инсулин? Это могут быть болезни инфекционного и хронического течения, которые ведут к ослаблению организма, понижают иммунитет. На количестве гормона неблагоприятно отражаются:
- стрессы;
- неврозы;
- неврологические болезни.
стрессовое состояние
В кровеносном русле может недоставать гормона, при этом насыщенность глюкозы расти не будет. Это указывает на проблемы эндокринной структуры поджелудочной железы, что требует консультации эндокринолога.
Процесс выработки гормона нарушается при наличии тех или иных заболеваний поджелудочной железы. В частности, панкреатит приводит к изменению тканей органа. В результате воспаления клетки, отвечающие за выработку ферментов и гормонов, гибнут, и их замещает соединительная ткань.

Если вы заметили у себя симптомы изменения уровня инсулина в крови, обязательно посетите врача.
В результате возникает не только внешнесекреторная недостаточность (проблемы с выработкой пищевых ферментов). Поджелудочная железа и инсулин оказывается неспособна вырабатывать в нужном количестве.
Однако не у всех пациентов патология развивается именно в такой последовательности. Бывает так, что пациенты, которым уже поставили диагноз «диабет второго типа», начинают страдать панкреатитом.
Повышенную выработку могут провоцировать различные факторы:
- нерегулярное и несбалансированное питание, изобилующее простыми углеводами;
- повышенные физические и психические нагрузки;
- ожирение;
- дефицит витамина Е и хрома.
Уровень гормона может подняться из-за болезней поджелудочной железы (речь идет о нарушении эндокринной функции органа), печени и опухолей в брюшной полости, а также при наступлении беременности. Низкие показатели могут говорить как о банальном физическом истощении (сильной усталости), так и о начале диабета.
За нехваткой инсулина стоит гибель синтезирующих его бета-клеток из-за атак собственной иммунной системы. При недостатке гормона поджелудочной железы инсулина клетки не имеют возможности впитывать глюкозу, а уровень сахара в крови продолжает оставаться гораздо выше допустимых норм.
Виды промышленного гормона
Виды инсулина классифицируются по нескольким признакам: степени очистки, виду животного, длительности действия и др.
Человеческий инсулин и его аналоги, полученные с помощью генной инженерии, являются более подходящими для применения в заместительной терапии, чем препараты животного происхождения.
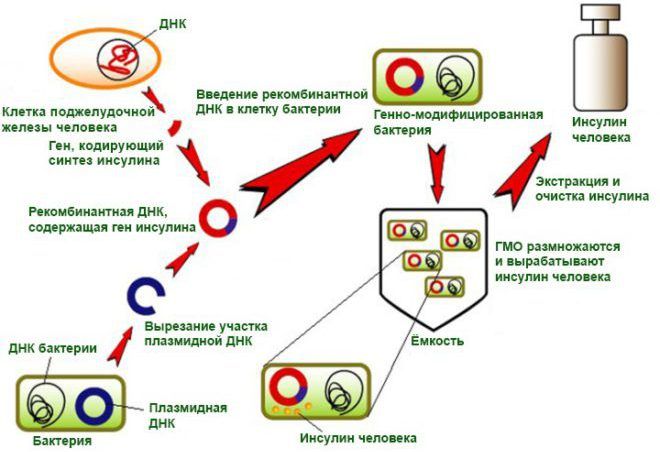
По длительности воздействия выделяют такие виды инсулина:
- Быстродействующий. Начинает воздействие в течение 5 минут после введения. Пиковый эффект наступает через 60-90 минут. Как правило, его вводят вместе с «длительным» гормоном непосредственно во время еды. Препараты этого типа – «Инсулин Хумалог», «Ново-Рапид» и др.
- Короткий. Первый эффект этого типа инсулина наступает через полчаса. Он вводится перед едой. К коротким относятся препараты «Монодар Хумодар», «Инсулин Актрапид».
- Средней длительности. Обычно используется в комбинации с «быстрыми» типами гормона. Сам по себе способен контролировать концентрацию глюкозы крови до половины дня. Препараты этого типа – «Протафан» (человеческий инсулин), «Инсулин Новомикс» и др.
- Гормон длительного воздействия. Действует на протяжении всего дня, однако эффект наступает через наибольшее время после введения, поэтому его необходимо комбинировать с «быстрыми» типами гормона. К гормонам длительного воздействия относят «Монодар Лонг», «Инсулин Лантус» и др.
Основные причины инсулиновой недостаточности
Нормальная поджелудочная железа вырабатывает около 200 единиц инсулина в сутки. При нарушениях её функционирования синтез гормона может существенно снизиться или полностью прекратиться. Глюкоза, поступающая с пищей, будет накапливаться в крови, не преобразуясь в гликоген – запасной источник энергии, откладывающийся в печени и мышцах. А это прямой путь к развитию сахарного диабета.
Если к диабету I типа (инсулинозависимому) приводят врождённые патологии поджелудочной железы или аутоиммунные расстройства, то приобретению инсулиновой недостаточности способствуют несколько факторов.
- Несбалансированное питание: синтез гормона нарушается при недостатке белков в рационе и при дефиците цинка, марганца и железа в употребляемых продуктах питания.
- Атеросклероз сосудов, при котором ухудшается кровообращение в поджелудочной железе и её нормальная работа.
- Острые и хронические воспаления поджелудочной железы (панкреатит).
- Нарушения образования ферментов.
- Злоупотребление продуктами, содержащими большое количество простых углеводов (сладости, изделия из муки высшего сорта).
Все факторы, которые могут привести к недостаточной выработке инсулина так или иначе связаны с неправильным питанием. Чтобы избежать проблем с поджелудочной железой и помочь её нормальному функционированию, необходимо придерживаться несколько правил.
Продукты, способствующие выработки инсулина
Регулярное включение в рацион полезной для работы поджелудочной железы пищи может нормализовать выработку инсулина и стать хорошим средством профилактики диабета. Употребление некоторых продуктов способствует также очищению органа от шлаков и токсинов, что имеет большое значение для его полноценного функционирования.
Продукты питания не должны рассматриваться в качестве альтернативы назначенным врачом лекарственных препаратов для выработки инсулина: они не заменяют медикаментозное лечение, а помогают поддержать функционирование организма.
Яблоки
Яблоки содержат большое количество витаминов, минеральных веществ, пектина и органических кислот. Входящие в состав фрукта вещества принимают участие в синтезе инсулина, нормализуют пищеварение и растворяют накопленные отложения шлаков в организме. Специалисты советуют принимать сладкие зелёные сорта яблок.
Для стимуляции работы поджелудочной железы полезен яблочный сок, который можно выпивать до трёх литров в день.
Для людей с инсулиновой недостаточностью, страдающих ожирением, рекомендуется лечение яблочным уксусом. Благодаря фруктовым кислотам, употребление уксуса снижает тягу к сладкому и расщепляет жировые клетки, выводя их из организма. Принимать по 2 ст.л. уксуса, растворённого в стакане воды, 3 раза в день во время еды в течение двух недель.
Клюква
Содержит много витаминов и минеральных солей. Лидер по количеству марганца среди растительной пищи. Употребление свежих или замороженных ягод и клюквенных морсов оказывает благотворное влияние на поджелудочную железу, улучшает кровообращение, нормализуя её деятельность. Рекомендуется ежедневно съедать 0,5 стакана ягод или выпивать до 1 л клюквенного морса.
Чтобы приготовить морс с максимальным сохранением всех его полезных свойств, нужно размять ягоды и залить их кипячёной водой, охлаждённой до 500 С (стакан клюквы на 1 л воды). Настоять в течение 3-4 часов. Вместо сахара можно положить немного мёда.
Орехи
Орехи богаты полиненасыщенными жирными кислотами омега-3, предупреждающими атеросклероз сосудов. Вкупе с большим количеством магния, марганца, белка и клетчатки орехи незаменимы в диетическом рационе больных с инсулиновой недостаточностью и сахарным диабетом.
Для оздоровительного эффекта достаточно съедать ежедневно по горсти миндаля, арахиса или грецких орехов.
Сельдерей
Входящие в состав сельдерея вещества способствуют очищению организма, предупреждают атеросклероз и нормализуют деятельность поджелудочной железы. При инсулиновой недостаточности полезен сельдереевый сок – принимать его нужно по полстакана утром натощак. Он благоприятно действует на сосуды, улучшает пищеварение, активизирует деятельность поджелудочной железы.
Морская капуста
Полезны при недостаточной выработке инсулина морские водоросли. Кобальт, марганец и цинк, содержащиеся в их составе, предотвращают нарушения в работе поджелудочной железы, способствуют синтезу гормона.
Ламинарию добавляют в салаты, каши, овощные блюда или используют измельчённые сушёные водоросли вместо соли.
В овсе содержатся ценные липотропные компоненты и ферменты, способствующие улучшению пищеварения. Зерновая культура обладает отличными абсорбирующими и детоксикациоными свойствами. За счёт очищающего действия на организм употребление овсяной каши или настоя улучшает функционирование поджелудочной железы. В лечебных целях применяют только неочищенный овёс (хлопья быстрого приготовления практически лишены полезных свойств).
Для помощи работе поджелудочной железе специалисты по естественному оздоровлению организма советуют принимать овсяное молочко.
Готовится оно по следующему рецепту:
- 100 г овса помыть проточной водой и залить в кастрюле 1,5 л воды.
- Поставить на плиту, довести до кипения и варить в течение часа на медленном огне.
- Перемолоть размягчённый овёс прямо в кастрюле с помощью блендера.
- Варить ещё 20 минут.
- Откинуть отвар на мелкое сито, слив жидкость (это и есть лечебное овсяное молочко).
Принимать отвар нужно по полстакана три раза в день до еды. Хранить в холодильнике не более двух суток.
Как образуется и действует гормон железы?
Итак, какие клетки поджелудочной железы вырабатывают инсулин? Синтез гормона осуществляется бета-клетками. Их еще называют панкреатическими островками либо островками Лангерганса.
Механизм образования гормона в организме относительно простой. Он начинает активно продуцироваться, когда возрастает количество углеводов в биологической жидкости. Любая еда, поступающая в желудок, запускает процесс синтеза гормонального вещества. Пища может быть белковой, растительной, жирной – не только углеводной. Когда человек плотно покушал, то концентрация гормона растет. На фоне голода – падает.